Estimados todas/os/es
En primer lugar quisiera pedir perdón a todos los físicos, ingenieros y químicos por la entrada de hoy. Voy a realizar muchas simplificaciones, pero la idea no es ilustrar a los lectores con mis conocimientos sino darles una herramienta útil frente a las noticias que saldrán, en primer lugar, en la prensa internacional y, luego cuando sean traducidas, en la prensa española. Todas ellas, interesadamente filtradas desde Maranello y/o Shell, sobre un nuevo carburante que hará ganador a Ferrari. Este año el termino bio-carburante está en horas bajas, la crisis económica hace que el termino bio o eco ya no nos excite como el año pasado, pero nos pondrán otro adjetivo sugerente y vacuo.
A las alturas del año que estamos todavía no sabemos muy bien cómo será la normativa del año 2012, sobre los distintos aspectos de la aerodinámica de los coches (legales, alegales, ilegales). Pero en el caso de las gasolinas, la legislación está totalmente cerrada desde hace muchos años y lo seguirá al menos hasta el 2015. El artículo 19 de las regulaciones técnicas de la Formula Uno es el encargado de esclarecer el tema de la gasolina (fuel) y como pueden comprobar tanto en 2011 como en 2014 son exactamente el mismo, palabra por palabra, incluyendo comas y, si me lo permiten, hasta en los errores tipográficos.
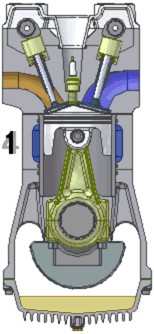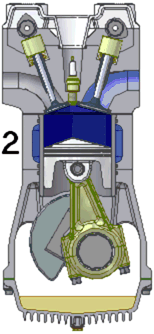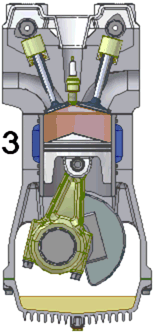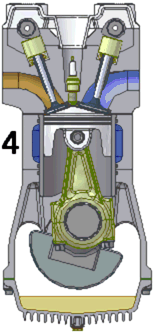
Para entenderlo bien, aunque solo sea un poco, empecemos desde el principio (¡Ojo! Con un montón de simplificaciones pero sin faltar a la verdad profunda de las cosas) ¿Qué ocurre en un coche para que se mueva? Pues lo más sencillo es decir que la energía que tienen ciertas moléculas (ΔG) se transforma por culpa de una reacción química en energía cinética (ΔEc), en movimiento de algo. En el clásico motor de cuatro tiempos en la etapa 3 (que pueden ver a la izquierda) tiene lugar la reacción química, de forma explosiva.
La reacción que tiene lugar es una reducción-oxidación, comúnmente llamada combustión. Y en ella, un carburante que ha de ser gasolina, según el apartado 19.3, se oxida con el oxigeno del aire [nitrógeno (78%), oxígeno (21%), agua (0-7%)], según la norma 19.5. Luego ya tenemos fijados varios parámetros que no podemos mover. Primero, el comburente ha de ser, por narices, el oxigeno del aire, lo que impide usar cualquier otro compuesto oxidante del conjunto del arsenal que poseen los químicos orgánicos actualmente (¡Una pena!).
¿Y qué es la gasolina? Pues es una mezcla de compuestos orgánicos, definida en el apartado 19.2 (alcanos, alquenos, alquinos y sistemas aromáticos). Lo importante es que todos son compuestos que contienen exclusivamente átomos de carbono y de hidrogeno, y la única diferencia es la presencia de enlaces simples o múltiples, entre los átomos de carbono. Incluso la cantidad de cada uno de estos compuestos, presente en la mezcla que llamamos gasolina, está establecida con límites muy estrictos, y con el protocolo y el aparato/técnica que se debe utilizar para saber si se cumple la norma 19.4.1. Solo decir que la técnica GCMS es la técnica de separación de productos por cromatografía de gases con un detector de espectrometría de masas. Para los profanos, solo decir que es el aparatito que sale con muchas lucecitas en series como CSI y que los técnicos miran en una pantalla de televisión y dicen un nombrajo raro que luego traducen a … pintura de coches, o cualquier otra cosa. Hay que recordar, también, que el error de la técnica es pequeñísimo, puede llegar a menos del 0.0001%, pero la FIA en su benevolencia permite un 0.1% de error. Ante la duda que le pregunten a Contador, y a su médico, sobre la sensibilidad de este método.
19.4.1 The composition of the petrol must comply with the specifications
detailed below
|
||||
Component
|
Units
|
Min
|
Max
|
Test
Method
|
Aromatics
|
wt%
|
40*
|
GCMS
|
|
Olefins
|
wt%
|
17*
|
GCMS
|
|
Total di-olefins
|
wt%
|
1.0
|
GCMS
|
|
Total styrene and alkyl derivatives
|
wt%
|
1.0
|
GCMS
|
|
*
Values corrected for fuel oxygen content.
|
||||
Según lo anteriormente citado la reacción general de la etapa 3 es, simplificando el combustible o gasolina a un alcano lineal simple [para cualquier otro tipo de compuesto orgánico lo único que varía es la letra n y/o el número de enlaces (líneas que puedes ver entre las letras -) entre carbonos (C)], la que sigue:
La energía de la reacción, o energía de Gibbs depende de dos factores. El primero es la entalpia (ΔH), y ese valor solo depende de los enlaces que se rompen y se crean en la reacción. Como el oxigeno (O2) es el comburente por ley y las gasolinas, mezclas de compuestos orgánicos, solo tienen enlaces carbono-carbono o carbono-hidrógeno, siempre se rompen los mismos enlaces y siempre se crean los mismos enlaces, luego desde el punto de vista de la entalpia, siempre se obtiene la misma energía. Y, como corolario, siempre se obtiene la misma velocidad (Δv), siendo redundante, el resultado es una constante.
Alguien con pensamientos aviesos debería preguntar por el segundo término ¿Qué pasa con TΔS? Ese es el termino de la entropía, del caos, del desorden (o de la suerte, como ya explique en alguna otra entrada) y depende, a groso modo, en nuestro caso del estado físico de los reactivos y los productos. En concreto, añadimos un liquido (vaporizado, pero liquido) y un gas y obtenemos solo gases. Y siempre es igual. Luego es constante.
Según lo anterior, para mejorar el rendimiento de los motores deberíamos cambiar la naturaleza del combustible o del carburante, pero eso está prohibido por ley. Una vez expuesta la ley, alguien podría pensar en hacer la trampa ¿Y si añadimos una pequeña cantidad de algo que cambie alguno de esos términos (entropía o entalpia de la reacción)? Si has pensado eso es que eres aficionado al aeromodelismo, y sabes que si alimentas un motor con metanol (CH3OH) y/o nitrometano (CH3NO2) el resultado es espectacular, comparándolo con el de la gasolina.
Si pensamos en algo que transfiera mucha energía y genere muchos gases de forma instantánea debemos fijarnos en los explosivos ¿Qué tal añadir algún explosivo a las gasolinas? A parte del problema de seguridad, veremos que es imposible. Los explosivos típicos, y tópicos, aparecen a continuación. Si se fijan bien, todos se caracterizan por tener átomos de nitrógeno (N), que al final de las reacciones terminan siendo el gas nitrógeno (N2). En algunos casos, podemos distinguir muy bien la agrupación nitro (NO2), que es ideal porque sirve de fuente oxidante (comburente) de la parte carbonada del explosivo. O lo que es lo mismo, estos últimos compuestos llevan puestos encima su propio aire para no necesitar añadir nada más en la famosa reacción del principio (¡Ojo que alguno de ellos se utiliza en medicina!).
Lo siento, pero la adición de compuestos nitrogenados, que fue ensayada en los años ochenta con el uso de nitrometano, está totalmente prohibida. Pero no solo eso, sino que en la norma 19.3 aparece la cantidad máxima de nitrógeno que puede haber en la gasolina (0.5 gramos por cada kilogramo), y nos dicen cómo medirlo (a través de un análisis elemental según las normas ASTM D 4629). Y encima el apartito que lo mide puede llegar a tener un error de 0.000003 gramos por kilo (¡Vamos que de engañar, na’ de na’!).
19.3 The only
fuel permitted is petrol having the following characteristics
|
||||
Property
|
Units
|
Min
|
Max
|
Test Method
|
(RON+MON)/2
|
87.0
|
ASTM D 2699/D 2700
|
||
Oxygen
|
wt%
|
3.7
|
Elemental Analysis
|
|
Nitrogen
|
mg/kg
|
500
|
ASTM D 4629
|
|
Benzene
|
wt%
|
1.0
|
GC-MS
|
|
RVP
|
kPa
|
45
|
60*
|
EN13016-1
|
Lead
|
g/l
|
0.005
|
ASTM D 3237
|
|
Oxidation Stability
|
minutes
|
360
|
ASTM D 525
|
|
Sulphur
|
mg/kg
|
10
|
EN ISO 20846
|
|
Electrical conductivity
|
pS/m
|
200
|
ASTM D 2624
|
|
Final Boiling Point
|
ºC
|
210
|
ISO 3405
|
|
Distillation Residue
|
%v/v
|
2.0
|
ISO 3405
|
|
* The maximum RVP may rise to
68kPa if a minimum of 2% bio-methanol and/or bio-ethanol are included in the
fuel.
|
||||
La norma 19.4.4 obliga a utilizar un mínimo de 5.75% de compuestos orgánicos que provengan de seres vivos, y no se admiten compuestos nitrogenados (¿Por qué será?).
Todavía nos queda un aspecto relacionado con la gasolina que deberíamos tratar. Y no es otro que el octanaje. En la fase 2, del motor clásico, el pistón sube comprimiendo a la mezcla reactante (gasolina vaporizada y aire en exceso) hasta el punto máximo que viene dado por la compresión de esta mezcla, donde estalla. Queda meridianamente claro que la mayor eficacia del proceso se obtiene cuando se ajusta el recorrido del pistón con la compresibilidad de la mezcla reactante ¿Y de que depende esta compresibilidad sin explosión? Pues depende de varios factores, pero uno de ellos es la naturaleza del compuesto orgánico que hay en la gasolina.
La capacidad antidetonante de un carburante ante la compresión es lo que vulgarmente llamamos octanaje. Las medidas de distintos compuestos mostraron que 2,3,4-trimetilpentano (también llamado isooctano, por la gentucilla de los químicos orgánicos) era un compuesto que se podía comprimir fuertemente y no presentaba autodetonación, por lo que se le dio el valor de 100, o número de octano (N. O.). Por el contrario el heptano, otro alcano, mostró una autodetonación muy alta por lo que se la asigno el valor de 0. Según estas definiciones, deberíamos saber que una gasolina de 95 octanos es aquella que se comporta como una mezcla 95% de isoooctano y 5% de heptano. Lo ideal es comprimir, a la gasolina, lo máximo posible para que el motor sea lo más pequeño posible. Y que el proceso de expansión sea lo más grande posible, ya que en ese movimiento es cuando transferimos la energía de Gibbs de la reacción a energía cinética (movimiento del pistón). Llegados a este punto alguien podría pensar en utilizar solo isooctano como combustible, pero por norma está prohibido y hay que utilizar mezclas ¿Pero es posible subir el octanaje con un aditivo? La respuesta la saben todos, sí. Los más mayores aun recordarán el usar gasolina con plomo (lead). La adición de pequeñas dosis de tetraetilplomo (entorno a 0.15 gr/l) aumentaba el octanaje cerca de cuatro unidades. Pero en la norma 19.3 podemos ver que no se puede añadir este antidetonante. Eso no quiere decir que no se utilicen otros, como 2-etoxy-2-metilpropano, o su primo 2-metoxi-2-metílpropano, ambos con números de octano muy altos. Incluso se suelen añadir alcoholes, como el etanol o metanol, anquen estos no son tan efectivos. En todo caso, su adición no es discrecional, ya que la cantidad máxima de oxigeno (O) que puede tener una gasolina es del 3.7% en masa.
Pero es que el octanaje también está limitado por el cociente (RON + MON)/2, que no puede bajar de 87. El RON es el acrónimo de Research Octane Number, o lo que es lo mismo el octanaje que se obtiene en un motor con un régimen bajo y numerosas aceleraciones, y es el númerito mágico que aparece en nuestras gasolineras. El MON es el acrónimo de Motor Octane Number, o lo que es lo mismo el octanaje que se obtiene con un motor en régimen y conducción regular (estático).
Confió que, con esta entrada tan larga, les haya dado herramientas suficientes para saber que la gasolina es lo único que no ha cambiado en la F1 desde finales de los ochenta y que permanecerá sin cambio, y sin posibilidades de hacer trampa, durante los próximos años.





9 comentarios:
Por fin alguien me aclara brevemente, que el equipo Red Bull no utiliza refrescos para ganar pontencia. Ahora ya no me queda duda, el genio es Newey, y no Dietrich Mateschitz como suponía.
UN SALUDO
Hola Rafael,
Estoy contigo que el genio es Newey, y gracias por lo de "brevemente" (¿?).
Un cordial saludo
Buenas tardes Primo.
Como siempre superandote, ademas en epoca de humo siempre esta bien conocer estos aspectos desconocidos por el gran publico.
Un saludo.
Hola Fourier,
Esa era la idea fundamental. Que la gente conozca una parte importante de la verdad para que pueda discernir qué es lo que lo he están ofreciendo como noticia.
Un cordial saludo
Hola Primo de anónimo:
Es que había que ponerle un tonillo de humor a este comienzo de temporada. Por cierto, que no lo mencioné, excepcional la explicación. Como siempre, muchas gracias.
UN SALUDO
De nuevo una entrada muy interesante y documentada. Aunque no venga totalmente al caso me gustaría compartir un pensamiento, esta mañana mientras leía una prueba del nuevo motor Ecoboost de Ford de 1 litro, 3 cilindros y 125CV, volvía a la reflexión que siempre me hago. ¿No sería mucho mejor un motor de 4 cilindros turbo de 1 litro e incluso un 2-3 cilindros biturbo y que los equipos tuviesen libertad en la evolución de los mismos?
Saludos!!!
Hola Rafael,
Y otra vez estoy totalmente de acuerdo. Y añadiría que no solo en el comienzo, sino en la parte media y en el final de todas las temporadas se necesita mucho humor. La vida es mucho más bonita con un poquito de humor diario ¿No lo crees así?
Hola VivaMansell,
Siguiendo tu hilo argumental. Estuve leyendo que, en Le Mans, Audi iba a competir con coches con motores híbridos (los Audi diesel ya han ganando esta carrera) ¿No sería muy retador para los ingenieros (y para las marcas de coches normales) el poder competir con motores diesel o híbridos? Tengo la extraña sensación que cada día más la F1 es un zoológico de dinosaurios de cera.
Saludos a ambos
Hola Primo.
Maravillosa explicacion de lo que es ese liquido que vale tanto dinero.Pero despues de tu maravilosa entrada me asalta una duda..en la F1 que utilizan 95 o 98 octanos...je,je
Hola Jaume,
Pues la verdad es que ni ellos mismos quieren saberlo.
Saludos
Publicar un comentario